Governo federal assina contrato para 10 milhões de doses da vacina Sputnik
Produto russo ainda não tem aprovação pela Anvisa; caixas devem começar a ser entregues em abril
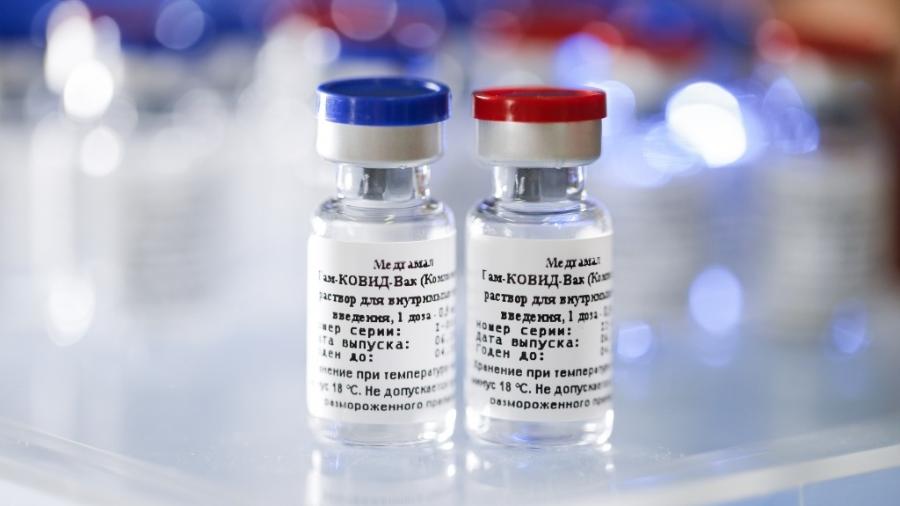
O Ministério da Saúde formalizou nesta sexta-feira (12) um contrato para receber 10 milhões de doses da vacina russa Sputnik V. De acordo com a pasta, o imunizante será entregue ao longo do segundo trimestre e as primeiras doses começam a chegar em abril.
A vacina será importada da russa pelo laboratório brasileiro União Química. “Chegamos a um bom entendimento para receber a Sputnik V, iniciado em ainda em agosto de 2020, quando a Rússia aprovou o uso desse imunizante para seus cidadãos. Aprofundamos essas negociações já no mês seguinte e agora temos mais um reforço para salvar vidas”, afirmou o secretário executivo do Ministério, Elcio Franco, por meio de nota.
No cronograma, 400 000 doses serão entregues até o final de abril, 2 milhões até o fim de maio e 7,6 milhões ao longo de junho. O item ainda não tem autorização para uso emergencial aprovado na Agência Nacional de Vigilância Sanitária (Anvisa).
A União Química informou para o Ministério da Saúde que pretende começar a fabricação da Sputnik V em território nacional, em unidades da farmacêutica localizadas em São Paulo e no Distrito Federal. A pasta informou que vai avaliar a concretização de um novo acordo comercial.
EFICÁCIA
A Sputnik V, de acordo com dados preliminares de uma pesquisa publicada no jornal científico The Lancet, conta com 91,6% de eficácia contra a Covid-19. A análise incluiu dados de 19 866 voluntários, que recebera a primeira e segunda dose do produto. 94% dos efeitos adversos apresentados foram reações leves, como dor no local de infeção e dor de cabeça.
VACINA DE OXFORD
Nesta sexta a Anvisa concedeu o registro definitivo para a vacina da AstraZeneca/Oxford. O primeiro imunizante a obter o registro definitivo no Brasil foi o da Pfizer.
A Anvisa anunciou também a aprovação do primeiro medicamento com indicação em bula para tratamento de pacientes infectados pela Covid-19, o antiviral Rendesivir. A mesma medicação, da biofarmacêutica americana Gilead Sciences, também foi aprovada no ano passado para uso como medicamento oficial para o tratamento da Covid-19 pela Food and Drug Administration (FDA), órgão norte-americano equivalente à Anvisa.





















