Vacina: Fiocruz pede registro emergencial para a Anvisa
É o segundo pedido do tipo nesta sexta (8); mais cedo, Butantan pediu análise da CoronaVac
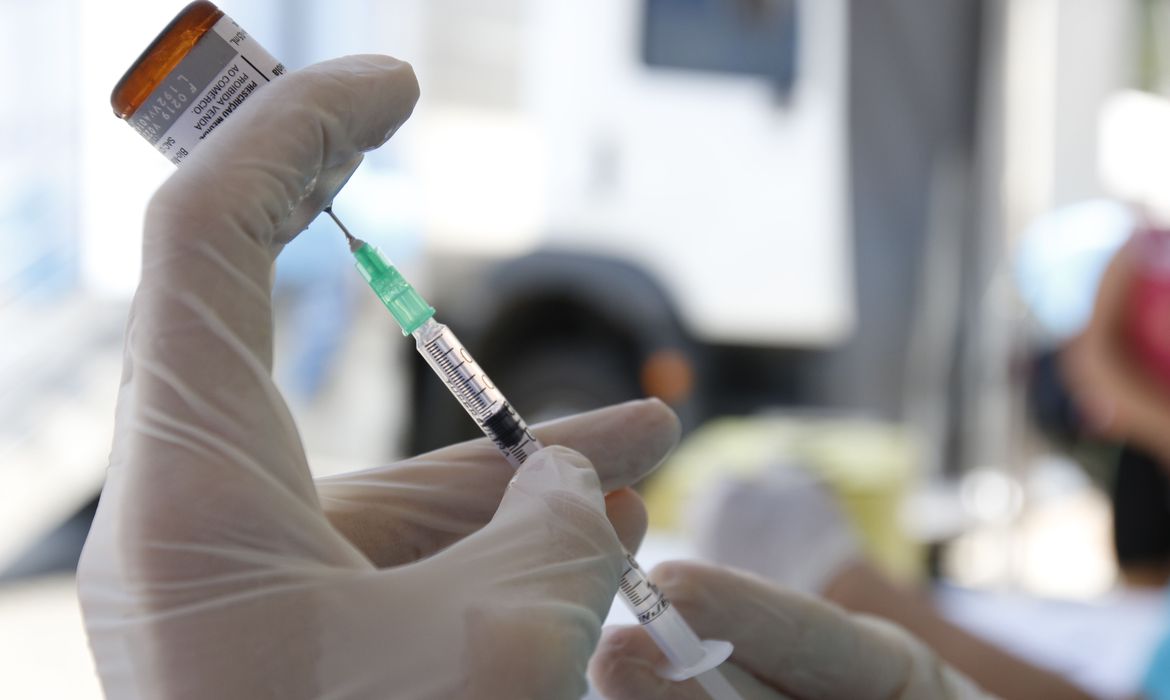
A Agência Nacional de Vigilância Sanitária (Anvisa) recebeu nesta sexta-feira (8) o pedido para uso emergencial da vacina desenvolvida pela Fundação Oswaldo Cruz em parceria com a Universidade de Oxford e a AstraZeneca.
De acordo com a Agência, a entidade solicitou a autorização para aplicar 2 milhões de doses prontas do imunizante, que serão importadas da Índia. O prazo para que a Anvisa analise o pedido é de dez dias.
O órgão afirmou em nota que a “análise é feita por uma equipe multidisciplinar, envolve especialistas das áreas de registro, monitoramento e inspeção”. A autorização emergencial permite que a vacina seja aplicada em grupos de risco: para a aplicação em massa é necessário o registro definitivo, que tem prazo de 60 dias.
CORONAVAC
Na manhã desta sexta a Agência recebeu também o pedido de uso emergencial da CoronaVac. O governo de São Paulo anunciou na quinta (7) que a taxa de eficácia da CoronaVac é de 78% para casos leves. Em casos graves, o índice atingiu a marca de 100%, protegendo totalmente contra a Covid-19. No Brasil, os testes envolveram 13 000 voluntários de vários estados.

 SEGUIR
SEGUIR
 SEGUINDO
SEGUINDO

 Parque Ibirapuera terá exposição imersiva da saga ‘Harry Potter’ em agosto
Parque Ibirapuera terá exposição imersiva da saga ‘Harry Potter’ em agosto Alexandre Birman cria coleção de sapatos inspirados em Lina Bo Bardi
Alexandre Birman cria coleção de sapatos inspirados em Lina Bo Bardi Dia Mundial da Criatividade tem atividades gratuitas espalhadas por SP
Dia Mundial da Criatividade tem atividades gratuitas espalhadas por SP Grife inspirada nos anos 2000 inaugura primeira loja em São Paulo
Grife inspirada nos anos 2000 inaugura primeira loja em São Paulo Conheça o polo de ecoturismo de SP, localizado em Parelheiros e Marsilac
Conheça o polo de ecoturismo de SP, localizado em Parelheiros e Marsilac






