Emílio Ribas inicia testes de vacina chinesa nesta quinta (30)
852 voluntários do hospital estão entre os 9 000 participantes da fase final da pesquisa
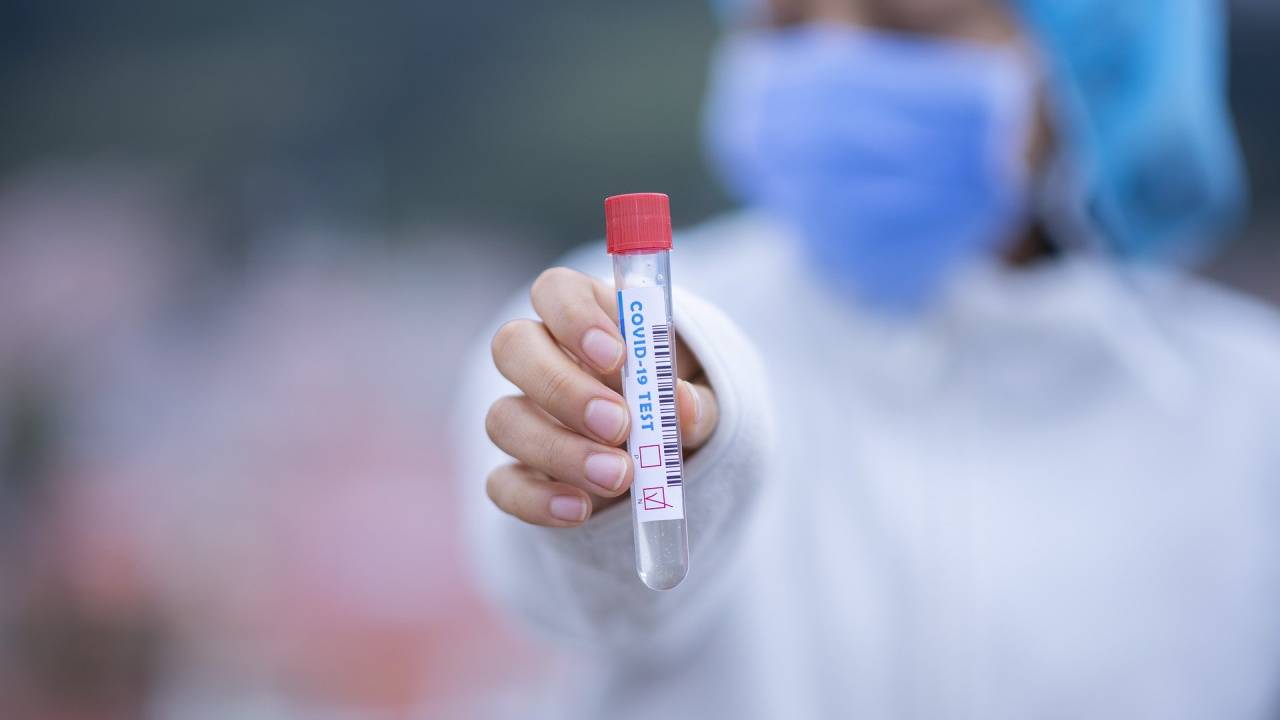
O Instituto de Infectologia Emílio Ribas iniciou os testes da nova vacina contra o coronavírus nesta quinta-feira (30). A primeira a receber a dose foi uma mulher que trabalha na área de enfermagem. Referência nacional para doenças infectocontagiosas, o hospital é o segundo centro de estudo a iniciar os testes da CoronaVac no Brasil.
O potencial imunizante está em fase final de pesquisa por meio de uma parceria entre o Instituto Butantan e a farmacêutica Sinovac Life Science. Dos 9 mil voluntários brasileiros, 852 são profissionais de saúde do Emílio Ribas. Na manhã desta quinta-feira (30), os testes também começaram no primeiro centro de estudo do interior de São Paulo, com 500 voluntários do HC (Hospital das Clínicas) da Faculdade de Medicina de Ribeirão Preto da USP.
A testagem coordenada pelo Butantan deve ser concluída entre o final de outubro e o início de novembro. No total, 12 centros de pesquisa foram selecionados no país. O Hospital das Clínicas da Faculdade de Medicina da USP foi o primeiro a aplicar a CoronaVac, no dia 21 de julho. No complexo do HC, são 890 voluntários.
Na sexta-feira (31), é a vez da Universidade Municipal de São Caetano do Sul e do Centro de Pesquisa e Desenvolvimento de Fármacos da UFMG (Universidade Federal de Minas Gerais).
O imunizante desenvolvido pela Sinovac Life Science é um dos mais promissoras do mundo porque utiliza tecnologia já conhecida e amplamente aplicada em outras vacinas. O Instituto Butantan avalia que sua incorporação ao sistema de saúde deva ocorrer mais facilmente.
O laboratório asiático já realizou testes em cerca de mil voluntários na China, nas fases 1 e 2. Antes, o modelo experimental aplicado em macacos apresentou resultados expressivos em termos de resposta imune contra o coronavírus.
A farmacêutica forneceu ao Butantan as doses da vacina para a realização de testes clínicos de fase 3 em voluntários no Brasil, com o objetivo de demonstrar sua eficácia e segurança.
Caso a vacina seja aprovada, a Sinovac e o Butantan vão firmar acordo de transferência de tecnologia para produção em escala e fornecimento gratuito pelo SUS. Os passos seguintes serão o registro do imunizante pela Anvisa (Agência Nacional de Vigilância Sanitária) e distribuição em todo o Brasil.
Abaixo, a relação dos 12 centros de estudo que vão participar da fase final de pesquisa da vacina contra o coronavírus:
Hospital das Clínicas da Faculdade de Medicina da USP
Instituto de Infectologia Emílio Ribas
Hospital das Clínicas da Faculdade de Medicina da USP de Ribeirão Preto
Universidade Municipal de São Caetano do Sul
Universidade Federal de Minas Gerais
Hospital Israelita Albert Einstein
Hospital das Clínicas da Unicamp
Faculdade de Medicina de São José do Rio Preto
Universidade de Brasília
Instituto Nacional de Infectologia Evandro Chagas de Fiocruz (RJ)
Hospital São Lucas da PUC do Rio Grande do Sul
Hospital das Clínicas da Universidade Federal do Paraná

 SEGUIR
SEGUIR
 SEGUINDO
SEGUINDO

 Parque Ibirapuera terá exposição imersiva da saga ‘Harry Potter’ em agosto
Parque Ibirapuera terá exposição imersiva da saga ‘Harry Potter’ em agosto Belo e Gracyanne se separam após mais de 15 anos de relacionamento
Belo e Gracyanne se separam após mais de 15 anos de relacionamento Museu do Ipiranga tem mostra gratuita de vídeos e distribuição de brinde
Museu do Ipiranga tem mostra gratuita de vídeos e distribuição de brinde Dia Mundial da Criatividade tem atividades gratuitas espalhadas por SP
Dia Mundial da Criatividade tem atividades gratuitas espalhadas por SP Aos 80 anos, HC aposta em pesquisas e inovação para se manter relevante
Aos 80 anos, HC aposta em pesquisas e inovação para se manter relevante






